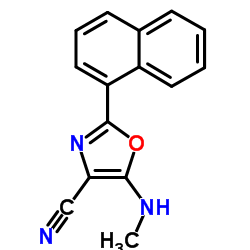
| 描述 |
ML351是一种有效且高度特异的15-LOX-1抑制剂,IC50为200 nM。与相关同功酶5-LOX、血小板12-LOX、15-LOX-2、绵羊COX-1和人COX-2相比,ML351表现出极好的选择性(>250倍)。ML351在T1D非肥胖糖尿病小鼠模型中预防血糖异常并降低β细胞氧化应激[2]。
|
| 相关类别 |
|
| 体外研究 |
ML351(1-50μM;24小时)对细胞凋亡没有有害影响(通过半胱天冬酶活性测定)[2]。ML351(10-50μM;24小时)在体外T1D模型中保护小鼠胰岛。暴露于促炎细胞因子的胰岛在2.5 mM葡萄糖下胰岛素释放增加,在25 mM葡萄糖下胰岛素释放受损。然而,ML351使2.5 mmol/L葡萄糖下的胰岛素分泌恢复到控制水平,与单独使用促炎细胞因子治疗相比,25 mM葡萄糖下的胰岛素释放显著改善[2]。ML351在体外逆转促炎细胞因子对小鼠胰岛ROS生成的刺激[2]。
|
| 体内研究 |
ML351(0-48毫克/千克;在STZ系列开始之前和最后一剂STZ后5天结束)在STZβ细胞损伤模型中保护糖尿病的发展。与对照组相比,24 mg/kg(M24)+STZ组的ML351体重减轻明显减少。M24几乎可以完全防止高血糖。但M48和M0在研究的第9天表现出明显的高血糖,并且显著损害了GTT[2]。ML351(腹腔注射;0-24mg/kg;每日2周)可改善血糖控制,显著减少胰岛炎。NOD小鼠中β细胞死亡的减少可能通过减轻死亡β细胞释放的趋化信号而导致胰岛炎的减少。与NOD+M0动物相比,NOD+M24动物的血糖控制有所改善[2]。动物模型:9周龄雄性C57BL/6J小鼠[2]剂量:0mg/kg;24mg/kg;48mg/kg;给药:在STZ系列开始前和最后一剂STZ后5天结束时腹腔注射结果:在模拟T1D炎症的STZβ细胞损伤模型中防止糖尿病的发展。动物模型:雌性NOD小鼠在12至24周龄期间发生自发性自身免疫性糖尿病[2]剂量:0 mg/kg;24mg/kg;48mg/kg;给药:在STZ系列开始前和最后一剂STZ后5天结束时腹腔注射结果:对NOD小鼠早期血糖恶化有保护作用。
|
| 参考文献 |
[1]. Thomas Gaberel, et al. Impact of 12/15-Lipoxygenase on Brain Injury After Subarachnoid Hemorrhage. Stroke. 2019 Feb;50(2):520-523. [2]. Ganesha Rai, et al. Discovery of ML351, a Potent and Selective Inhibitor of Human 15-Lipoxygenase-1 [3]. Marimar Hernandez-Perez, et al. Inhibition of 12/15-Lipoxygenase Protects Against β-Cell Oxidative Stress and Glycemic Deterioration in Mouse Models of Type 1 Diabetes. Diabetes. 2017 Nov;66(11):2875-2887.
|