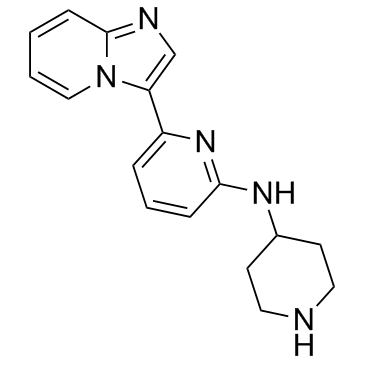
1042224-63-4
| 中文名 | IRAK抑制剂1 |
|---|---|
| 英文名 | 6-imidazo[1,2-a]pyridin-3-yl-N-piperidin-4-ylpyridin-2-amine |
| 英文别名 |
CS-0603
IRAK inhibitor 1 |
| 描述 | IRAK inhibitor 1 是一种有效的 IRAK-4 抑制剂,IC50 为 216 nM,微弱抑制 JNK-1 和 JNK-2,IC50 分别为 3.801 μM 和 >10 μM。 |
|---|---|
| 相关类别 | |
| 靶点 |
IC50: 216 nM (IRAK-4), 3.801 μM (JNK-1), >10 μM (JNK-2)[1] |
| 体外研究 | IRAK抑制剂1在IRAK-4酶测定中具有显着的效力,但对JNK-1和JNK-2的活性很差[1]。 IRAK-4是IRAK系列的新成员,具有独特的功能特性。 IRAK-4是最接近Pelle的人类同源物。内源性IRAK-4以IL-1依赖性方式与IRAK-1和TRAF6相互作用,并且IRAK-4的过表达可以激活NF-κB以及丝裂原活化蛋白(MAP)激酶途径。最引人注目的是,与其他IRAK相比,IRAK-4依赖于其激酶活性来激活NF-κB。此外,IRAK-4能够使IRAK-1磷酸化,并且显性失活的IRAK-4的过表达阻断IL-1诱导的IRAK-1的激活和修饰,表明IRAK-4作为中心元件的作用。在IRAK-1上游的Toll/IL-1受体的早期信号转导中。 IRAK-4共享其他IRAK的结构域结构,并且能够激活类似的信号转导途径,即NF-κB和MAPK途径。它以IL-1依赖性方式快速且瞬时地与IRAK-1和TRAF6结合,但在功能上与IRAK-1无关。 IRAK-4是一种活性蛋白激酶,需要其激酶活性才能激活NF-κB。 IRAK-4可能作为IRAK-1活化剂在IRAK-1的上游起作用[2]。 |
| 参考文献 |
| 分子式 | C17H19N5 |
|---|---|
| 分子量 | 293.36600 |
| 精确质量 | 293.16400 |
| PSA | 54.25000 |
| LogP | 2.96200 |
| 储存条件 | 2-8℃ |