| 描述 |
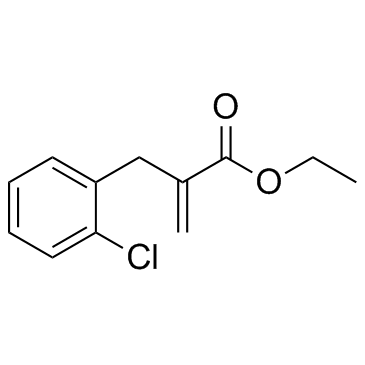
INF39 是不可逆的,没有细胞毒性的NLRP3 抑制剂。
|
| 相关类别 |
|
| 体外研究 |
INF39能够在10μM时显着抑制ATP-和奈斯克林诱导的IL-1β释放。 INF39可减少巨噬细胞中caspase-1的活化和焦磷酸化。 INF39不仅可以阻断NLRP3的激活,还可以阻断NF-κB通路。 INF39可能与半胱氨酸蛋白酶caspase-1活性位点中的Cys-SH残基反应,但不直接靶向caspase-1活性。 INF39能够在不影响细胞活力的情况下降低NLRP3的稳态(或基础)BRET信号,这意味着它可以干扰基础NLRP3构象。 INF39不会阻断NLRP3在检测到细胞内K +降低时所遭受的初始构象变化;然而,它影响NLRP3构象变化的第二步,其可能与受体的ATP酶活性相关并且不依赖于细胞内K +的减少。 INF39在不经历化学修饰的情况下到达肠上皮细胞。在吸收到上皮细胞后,它可能在粘膜上皮水平局部起作用[1]。
|
| 体内研究 |
口服INF39可减少用2,4-二硝基苯磺酸处理的大鼠的全身和结肠炎症。在INF39(12.5,25和50mg/kg)治疗下,在发炎的大鼠中观察到显着的体重增加。用DNBS治疗导致脾脏重量显着增加(+ 39.3%)。通过施用INF39显着降低这种增加(分别为12.5,25,50mg/kg时+2.2,+ 4.3和+ 4.8%)。用INF39抑制NLRP3炎性体复合物剂量依赖性地减弱结肠长度的减少(分别为12.5,25,50mg/kg时-19,-13和-8%)。用INF39处理的大鼠显示出宏观损伤评分的显着降低(12.5mg/kg时为4.7,35mg/kg时为3.1,50mg/kg时为2.8)。口服INF39可降低DNBS治疗大鼠的结肠髓过氧化物酶,IL-1β和TNF水平[1]。
|
| 激酶实验 |
将INF39(100μM终浓度,2%DMSO)加入到含有固定化NALP3蛋白的孔中,并在37℃下预孵育55分钟以模拟正常实验时间(预孵育15分钟+与ATP孵育40分钟);在对照孔中加入缓冲液和DMSO的混合物。在预孵育时间后,用反应缓冲液将孔重复三次,并在37℃下加入ATP(250μM)40分钟。用ADP-Glo-Assay [1]测量ADP形成。
|
| 动物实验 |
大鼠:将DNBS未处理的和DNBS处理的动物分配到以下处理组:INF39(12.5,25,50mg / kg /天)或地塞米松(DEX,1mg / kg /天)。将INF39和地塞米松分别悬浮在橄榄油和1%甲基纤维素中,并以0.2mL /大鼠的体积给药。 DNBS未处理的动物(对照组)和DNBS处理的大鼠(结肠炎组)接受药物载体作为对照。从药物治疗开始每天监测体重[1]。
|
| 参考文献 |
[1]. Cocco M, et al. Development of an Acrylate Derivative Targeting the NLRP3 Inflammasome for the Treatment of Inflammatory Bowel Disease.J Med Chem. 2017 May 11;60(9):3656-3671.
|